服務專區
Service
健康食品查驗登記概說
「健康食品管理法」於八十八年八月三日施行後,「健康食品」乙詞已成為法律名詞,法律上之定義為「具有保健功效,並標示或廣告其具該功效,且須具有實質科學證據,非屬治療、矯正人類疾病之醫療效能為目的之食品」。
食品(包括坊間所稱保健食品)未取得衛生福利部健康食品查驗登記許可證,而宣稱為「健康食品」或具健康食品之保健功效者,則依違反健康食品管理法,移送法辦,而坊間所稱之「保健食品」,其實就是一般食品,僅能做為營養補充,兩者並不相同。
核准通過之「健康食品」須於產品包裝標示健康食品、核准之證號、標章及保健功效等相關規定項目,但仍不得述及醫療效能、虛偽不實、誇張或超出許可範圍之保健功效。
查驗登記及管理
健康食品查驗登記係採雙軌制:
(一) 第一軌:個案審查
業者須檢具製程品管及各種實驗或科學驗證,向衛生福利部提出申請,經衛生福利部健康食品審議小組委員審查評估其安全無虞以及科學佐證之功效性,獲得通過,始取得健康食品許可證,所准許宣稱之保健功效範圍取決於個別產品所提出科學驗證之結果。
個案審查一般需耗時180個日曆天,審查費用250,000元整(初審80,000元整,複審170,000萬元整,不含領證費及檢驗費),通過審查的產品會給予健康食品標章(如下圖)及字號,於88年至102年7月22日所核發之字號為「衛署健食字號(衛署健食字第A00000號)」;自102年7月23日起,因「衛生署」改制為「衛生福利部」,故自該日後獲得健康食品審查通過之產品,證書字號改為「衛部健食字號(衛部健食字第A00000號)」。

(二)第二軌:規格標準審查
針對科學上已相當確知具有保健功效的成分開放規格標準審查,衛生福利部評估開放規格標準品項及其建議攝取量之四要件:1. 傳統長久供飲食經驗安全無疑慮、2. 功效機轉明確、3. 有效成分明確、4. 已建立有效成分之分析方法。產品成分符合衛生福利部公告之健康食品規格標準,由學理確立產品依建議攝取量具保健功效並且安全無虞,並提供申請產品符合公告之規格標準等檢驗報告,無需進行保健功效評估試驗及安全試驗。目前已公告的健康食品規格標準為魚油及紅麴兩項,凡獲得通過者,可宣稱之保健功效範圍均相同。如:魚油類產品可標示:「本產品可能有助於降低血中三酸甘油酯;其功效乃由學理得知,非由實驗確認」;紅麴類產品可標示:「本產品可能有助於降低血中總膽固醇;其功效由學理得知,非由實驗確認」。
規格標準審查型一般需耗時120個日曆天,審查費用80,000元整(不含領證費及檢驗費),通過審查的產品會給予健康食品標章(如下圖)及字號,於88年至102年7月22日所核發之字號為「衛署健食規字號(衛署健食規字第000000號)」;自102年7月23日起,因「衛生署」改制為「衛生福利部」,故自該日後獲得健康食品審查通過之產品,證書字號改為「衛部健食規字號(衛部健食規字第000000號)」。

通過審核的健康食品之製造、輸入許可證有效期限為五年。期滿仍須繼續製造、輸入者,應於許可證到期前三個月內申請中央主管機關核准展延之,但每次展延不得超過五年,逾期未申請展延或不准展延者,原許可證自動失效。
健康食品分類
目前公告之保健功效共13項:
- 胃腸功能改善
- 調節血脂功能
- 護肝功能
- 骨質保健功能
- 免疫調節功能
- 輔助調整過敏體質功能
- 不易形成體脂肪功能
- 調節血糖功能
- 輔助調節血壓功能
- 抗疲勞功能
- 延緩衰老功能
- 促進鐵吸收功能
- 牙齒保健功能
健康食品管理法令
衛生福利部已依據健康食品管理法,陸續訂定有關子法,包括:「健康食品管理法施行細則」、「健康食品申請許可辦法」、「紅麴健康食品規格標準」、「魚油健康食品規格標準」、「健康食品安全性評估方法」、「健康食品之保健功效評估方法(13項)」、「健康食品器具容器包裝衛生標準」、「健康食品原子塵放射能污染之安全容許量標準」、「健康食品殘留農藥安全容許量標準」、「健康食品衛生標準」及「健康食品工廠良好作業規範」等規定。至於健康食品管理法未規定者,則適用於食品衛生管理法相關規定。
健康食品 VS. 保健食品
「健康食品」原本是一日常用語(普通名詞,商業名詞),自健康食品管理法施行後,食品一定要經過衛生福利部審查通過後才能稱為「健康食品」,一般食品不得擅自標示或廣告為「健康食品」,或是具有健康食品之「保健功效」,而坊間所稱之「保健食品」,其實就是一般食品,僅能做為營養補充,兩者並不相同。
委託成功案例
| 一軌 | |||
|---|---|---|---|
| No. | 產品名稱 | 保健功效 | 核准字號 |
| 1 | 木糖醇+2無糖口香糖-蘋果薄荷 | 牙齒保健功能 | 衛署健食字第A00094號 |
| 2 | 木糖醇+2無糖口香糖-清涼薄荷 | 牙齒保健功能 | 衛署健食字第A00095號 |
| 3 | 頂級四物鐵飲料 | 促進鐵可利用率功能 | 衛署健食字第A00142號 |
| 4 | 納麴Q10膠囊 | 調節血脂功能 | 衛署健食字第A00173號 |
| 5 | 活力五味子錠 | 護肝功能 | 衛署健食字第A00223號 |
| 6 | 悠康-納麴Q10膠囊 | 調節血脂功能 | 衛部健食字第A00245號 |
| 7 | 櫻桃姬補鐵精華液 | 促進鐵可利用率功能 | 衛部健食字第A00263號 |
| 8 | 深海魚油薑黃+E膠囊 | 調節血脂功能 | 衛部健食字第A00268號 |
| 9 | 安怡TM長青高鈣奶粉 | 骨質保健功能 | 衛部健食字第A00291號 |
| 10 | 船井牛奶鈣魚膠原粉 | 骨質保健功能 | 衛部健食字第A00295號 |
| 11 | 安怡TM關鍵高鈣奶粉 | 骨質保健功能 | 衛部健食字第A00311號 |
| 12 | 安怡TM高鈣奶粉 | 骨質保健功能 | 衛部健食字第A00312號 |
| 13 | 好味粥 | 胃腸功能改善 | 衛部健食字第A00315號 |
| 14 | 膠原糖胺粉Plus | 骨質保健功能 | 衛部健食字第A00318號 |
| 15 | 樟芝人參滋補液 | 護肝功能 | 衛部健食字第A00320號 |
| 16 | 樟芝人參滋補液 | 抗疲勞功能 | 衛部健食字第A00320號 |
| 17 | L-137®植物乳酸菌膠囊 | 免疫調節功能 | 衛部健食字第A00322號 |
| 18 | L-137®植物乳酸菌膠囊 | 輔助調整過敏體質 | 衛部健食字第A00322號 |
| 19 | FIP100纖維粉 | 胃腸功能改善 | 衛部健食字第A00324號 |
| 20 | FIP100纖維粉 | 調節血脂功能 | 衛部健食字第A00324號 |
| 21 | FIP100纖維粉 | 調節血糖功能 | 衛部健食字第A00324號 |
| 22 | 倍熱®極纖錠 | 不易形成體脂肪功能 | 衛部健食字第A00332號 |
| 23 | 果寡糖順暢粉 | 胃腸功能改善 | 衛部健食字第A00338號 |
| 24 | 速美錠 | 不易形成體脂肪功能 | 衛部健食字第A00343號 |
| 25 | 欣可清膠囊 | 調節血脂功能 | 衛部健食字第A00347號 |
| 26 | 紅麴磷蝦油軟膠囊 | 調節血脂功能 | 衛部健食字第A00358號 |
| 27 | GSH 顧甘肽膠囊 | 護肝功能 | 衛部健食字第A00368號 |
| 28 | 田原香靈芝滴雞精 | 免疫調節功能 | 衛部健食字第A00375號 |
| 29 | 田原香靈芝滴雞精 | 抗疲勞功能 | 衛部健食字第A00375號 |
| 30 | 威瑪舒培活力錠 | 抗疲勞功能 | 衛部健食字第A00382號 |
| 31 | 金肽康五味子錠 | 護肝功能 | 衛部健食字第A00385號 |
| 32 | 健康3D紅麴+鉻雙效錠 | 調節血脂功能 | 衛部健食字第A00387號 |
| 33 | 健康3D紅麴+鉻雙效錠 | 調節血糖功能 | 衛部健食字第A00387號 |
| 34 | 維士比倍勁X水補給飲 | 抗疲勞功能 | 衛部健食字第A00389號 |
| 35 | 挺固錠 | 骨質保健功能 | 衛部健食字第A00390號 |
| 36 | 婕樂纖 纖飄錠 | 不易形成體脂肪功能 | 衛部健食字第A00394號 |
| 37 | 婕樂纖 纖飄錠 | 調節血脂功能 | 衛部健食字第A00394號 |
| 38 | 苷寳良®uSOLA紅麴植萃膠囊 | 護肝功能 | 衛部健食字第A00401號 |
| 39 | 新胺-水溶性殼醣胺 | 調節血脂功能 | 衛部健食字第A00402號 |
| 40 | 聚安堂納豆紅麴膠囊 | 調節血脂功能 | 衛部健食字第A00412號 |
| 41 | 氧甘寶錠 | 抗疲勞功能 | 衛部健食字第A00414號 |
| 42 | 氧甘寶錠 | 護肝功能 | 衛部健食字第A00414號 |
| 43 | 健行鈣樂飲 | 骨質保健功能 | 衛部健食字第A00417號 |
| 44 | 綠朔孅錠 | 不易形成體脂肪功能 | 衛部健食字第A00420號 |
| 45 | 勁亮神采錠 | 抗疲勞功能 | 衛部健食字第A00430號 |
| 46 | 谷穩錠 | 骨質保健功能 | 衛部健食字第A00438號 |
| 47 | BB神采速纖飲 | 抗疲勞功能 | 衛部健食字第A00439號 |
| 48 | 華陀旨樂清膠囊 | 調節血脂功能 | 衛部健食字第A00440號 |
| 49 | 枳椇子朝鮮薊複方錠 | 護肝功能 | 衛部健食字第A00441號 |
| 二軌 | ||
|---|---|---|
| No. | 產品名稱 | 核准字號 |
| 1 | 特級紅麴膠囊 | 衛署健食規字第000007號 |
| 2 | 健康純淨魚油膠囊 | 衛署健食規字第000013號 |
| 3 | 生活挪威深海魚油膠囊 | 衛署健食規字第000016號 |
| 4 | 安可健紅麴膠囊 | 衛署健食規字第000021號 |
| 5 | 益通麴紅麴膠囊 | 衛署健食規字第000022號 |
| 6 | 黃金魚油膠囊 | 衛署健食規字第000025號 |
| 7 | 頂級紅麴膠囊 | 衛署健食規字第000027號 |
| 8 | TS6®純淨紅麴膠囊 | 衛署健食規字第000028號 |
| 9 | 精粹紅麴隨手包 | 衛部健食規字第000051號 |
| 10 | 悠萃美佳魚油軟膠囊 | 衛部健食規字第000054號 |
| 11 | 如順健康魚油膠囊 | 衛部健食規字第000055號 |
| 12 | 天河賞健康魚油膠囊 | 衛部健食規字第000061號 |
| 13 | 伊美維達健康紅麴膠囊 | 衛部健食規字第000066號 |
| 14 | BHK’s深海魚油軟膠囊 | 衛部健食規字第000068號 |
| 15 | 北条博士-通醇精純魚油軟膠囊 | 衛部健食規字第000069號 |
| 16 | 速速清魚油軟膠囊 | 衛部健食規字第000070號 |
| 17 | 大醫生技紅麴膠囊 | 衛部健食規字第000072號 |
| 18 | 益健紅麴膠囊 | 衛部健食規字第000073號 |
| 19 | 優旨樂®深海魚油軟膠囊 | 衛部健食規字第000074號 |
| 20 | 2812機能魚油軟膠囊 | 衛部健食規字第000078號 |
| 21 | 菁萃高純度DHA魚油軟膠囊 | 衛部健食規字第000080號 |
| 22 | 大醫生技DHA+EPA TG型魚油膠囊 | 衛部健食規字第000081號 |
醫療器材查驗登記概說
依照藥事法第十三條規定,所稱醫療器材,係用於診斷、治療、減輕、直接預防人類疾病、調節生育,或足以影響人類身體結構及機能,且非以藥理、免疫或代謝方法作用於人體,以達成其主要功能之儀器、器械、用具、物質、軟體、體外試劑及其相關物品;藥事法第四十條規定,製造、輸入醫療器材,應向中央衛生主管機關申請查驗登記並繳納費用,經核准發給醫療器材許可證後,始得製造或輸入。藥事法規範的不僅是製造層面,醫療器材的輸入也在法律規範裡。換言之,即便是業者想要從國外進口輸入,也需事先向中央衛生主管機關申請許可證,始得進行後續作業,否則將面臨違反法規的風險。
醫療器材管理
醫療器材管理辦法是由主管機關依藥事法第十三條第二項規定訂定,也是醫療器材管理法規的核心,管理辦法所揭示的管理重點如下:
(一)療器材首重安全,故以「風險」程度,將其分為三個等級:
a. 第一等級(低風險)醫療器材,如:棉花棒、紗布、機械式輪椅、一般醫用口罩等。
b. 第二等級(中風險)醫療器材,例如:隱形眼鏡、血糖機、血壓計、體溫計、低週波治療儀等。
c. 第三等級(高風險)醫療器材,例如:血管支架、心律調節器等。
(二)醫療器材依據功能、用途、使用方法及工作原理,區分為十七大類。分類分級表可於衛福部網站查詢 前往查詢
(三)醫療器材的製造原則上應符合醫療器材優良製造規範的規定。
(四)以正面表列方式列出須於國內進行臨床試驗的醫療器材品項。
醫療器材許可證
衛生福利部食品藥物管理署核發醫療器材許可證,其核准字號如下:
(1)、衛部(署)醫器輸(壹)字第******號
(2)、衛部(署)醫器製(壹)字第******號
(3)、衛部(署)醫器陸輸(壹)字第******號
(4)、罕醫輸(製)第******號
(5)、衛部(署)醫器外製字第******號
若有許可證產品資訊的問題,可至衛生福利部食品藥物管理署網站之「醫療器材許可證資料庫」網頁查詢 前往查詢
確保食品對於人體無害且具有穩定的保健功效。因此必須根據產品特性進行功效性成份安定性實驗。
安定性報告需涵蓋以下部分:
- i. 方法專一性
- ii. 方法確效
- iii. 架儲期(保存期限)推算
安全評估主要係針對以往長期食用及製造加工之安全性作考量,包括食用目的、方式、製造加工方法、流程、最終產品形式及攝食量等均為分類之考慮因素。
| 健康食品類別與安性試驗要求 | |||||
|---|---|---|---|---|---|
| 安全性試驗項目 | 產品原料分類 | 第一類 傳統食用以通常加工形式供食者 |
第二類 傳統食用以非通常加工形式供食者 |
第三類 非傳統食用 |
第四類 非傳統食用含有致癌類似物 |
| 基因毒性 | 包括沙門氏桿菌回復突變試驗,中國倉鼠卵巢細胞染色體異變分析及生體內細胞小核分析 | ||||
| 28天餵食毒性試驗 | 評估連續投予試驗物質28天後是否具毒性反應 | ||||
| 90天餵食毒性試驗 | 評估連續投予試驗物質90天後是否具毒性反應 | ||||
| 致畸試驗 | 評估試驗物質是否對妊娠動物是否造成胎兒畸形 | ||||
| 慢性毒性/致癌性試驗 | 評估連續長期投予試驗物質是否具毒性及致癌可能性 | ||||
| 繁殖試驗 | 評估試驗物質是否具毒性及致癌可能性造成動物生長機能及對於子代之影響 | ||||
| 無須進行試驗 需進行試驗 | |||||
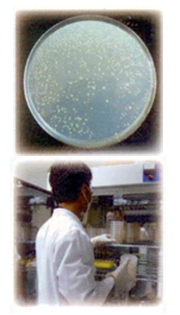
基因毒性-沙門氏桿菌回復突變試驗
利用試驗物質對沙門氏桿菌(Salmonella typhimurium)造成基因之回復突變情形,在代謝活化物存在與否的條件下(代謝活化物:S9混合物),判斷試驗物質是否對微生物細胞具有致變異性。
本服務提供5株測試菌株:TA97a、TA98、TA100、TA102、TA1535。利用平板培養法(plate incorporation)或是前置培養法(preincubation)測試。
沙門氏桿菌回復突變劑量測試Ranging Finding |
|
沙門氏桿菌回復突變測試-單一劑量Ames Test-Single Dose |
|
沙門氏桿菌回復突變測試Ames Test |
|
以上測試項目均為3重覆測試,測試範圍均包含
- With S9混合物測試
- Without S9混合物測試
- Positive control
- Negative control
- 測試相關結果報告
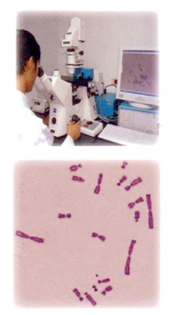
基因毒性-體外染色體變異分析
利用倉鼠卵巢細胞(CHO K1 cell)評估試驗物質是否會引發染色體結構之異常。藉由觀察200個分裂中期細胞,計算染色體或染色分體的結構變異種類及數量、變異細胞之頻率,及多套染色體(polyploid)的數目來鑑別試驗物質是否具有毒性。
細胞毒性測試Cytotoxicity Test |
|
染色體變異分析Chromosome Aberrations in CHO K1 Cells |
|
以上測試項目為2重覆測試,測試範圍均包含
- With S9混合物測試
- Without S9混合物測試
- Positive control
- Negative control
基因毒性-體內基因毒性分析
基因變異,包括點突變,或是各種染色體變異,導致基因功能異常。體外基因突變測試是利用試驗物質處理特定細胞株,是否產生致突變表現型(mutant phenotype)來鑑別。
細胞毒性測試Cytotoxicity Test |
|
體外小鼠淋巴瘤TK Assay In vitro mouse lymohoma -TK assay |
|
動物毒性試驗
以經口灌食/皮膚接觸/吸入/或其他途徑法給予試驗動物受是樣品,觀察動物的毒性反應。執行動物毒性試驗,需採集血液或血清,以進行血液相分類、血液凝固分析、血清生化分析等檢驗,最後進行大體解剖,摘取臟器秤重並肉眼檢查臨床病理症狀,並進一步製作病理組織切片及病理檢查,以做光學顯微鏡檢查,並完成藥物對各種臟器影響之組織病理評估報告。
急性毒性試驗Acute LD50 Toxicity Test |
|
亞(急)慢性毒性試驗Subacute Toxicity Test |
|
慢性毒性試驗Chronic Toxicity Test |
|
致癌試驗
試驗物質若為(1)需持續給藥6個月以上(2)可能引起致癌性(3)作用機制推測有致癌性(4)重複劑量毒性試驗有腫瘤生成現象(5)試驗物質成分或代謝產物長期滯留於組織中,產生局部組織作用或病理生理反應(6)基因突變試驗結果有致突變性存在者,應進行致癌試驗。
長期給予實驗動物受試化學物質,觀察動物出現腫瘤的數量及時間。動物致癌性試驗為人體長期接觸該物質是否引起腫瘤提供資料。
長期致癌試驗Carcinigenicity Study |
|
調節血糖功能
動物試驗
實驗設計:包含正常對照組及3個以上不同劑量組,每組至少8隻動物
遺傳性自發高血糖動物帶有遺傳性自發高血糖的動物:大(小)鼠 |
|
遺傳性自發高血糖動物以藥物誘發高血糖症狀,待一星期後,採血測量隔夜空腹(17~24小時)血糖值,若達或超過13 mM (230+10 mg %) 時,則視為有糖尿病:大(小)鼠 |
|
其他動物模式給予實驗動物STZ(65 mg/kg)加上Nicotinamide (230 mg/kg)。若達或超過13 mM (230+10 mg %) 時,則視為有糖尿病:大(小)鼠 |
|
人體試驗
實驗設計:包含正常對照及受試物組,受試人數每組至少20人。
|
血糖值偏高者或臨床上判定為輕微糖尿病症者且應本著自覺自願的原則 |
|
護肝功能
動物試驗
【針對四氯化碳誘導化學性肝損傷】
實驗設計:包含正常對照組、負控制組及至少2組劑量組,每組至少8隻動物
四氯化碳誘導化學性肝損傷四氯化碳誘導肝損傷前一星期即開始給予試驗樣品:大鼠 |
|
【常用止痛藥物乙醯胺基苯酚誘導之化學性肝炎損傷】
實驗設計:包含正常對照組、負控制組、正控制組及至少2組劑量組,每組至少10隻動物
常用止痛藥物乙醯胺基苯酚誘導之化學性肝炎損傷APAP誘導肝損傷前一星期即開始給予試驗樣品:小鼠 |
|
【應用硫代乙醯胺誘導肝纖維化之慢性肝損傷】
實驗設計:包含正常對照組、負控制組及至少2組劑量組,每組至少8隻動物
應用硫代乙醯胺誘導肝纖維化之慢性肝損傷TAA誘導肝損傷前一星期即開始給予試驗樣品:大鼠 |
|
【針對應用酒精液態飼料誘導酒精性脂肪肝】
實驗設計:包含正常對照組、負控制組及至少2組劑量組,每組至少10隻動物
針對應用酒精液態飼料誘導酒精性脂肪肝Lieber-DeCarli流質酒精飼料誘導肝損傷前一星期即開始給予試驗樣品:小鼠 |
|
【針對高脂飼料誘導非酒精性脂肪肝】
實驗設計:包含正常對照組、負控制組及至少2組劑量組,每組至少10隻動物
針對高脂飼料誘導非酒精性脂肪肝高脂飼料誘導肝損傷前一星期即開始給予試驗樣品:小鼠 |
|
免疫調節功能
動物試驗
實驗設計:實驗組別每組至少10隻動物
針對非特異性免疫反應小鼠 |
|
針對特異性免疫反應小鼠 |
|
人體試驗
實驗設計:與動物的評估近似
針對非特異性免疫反應 |
|
針對特異性免疫反應 |
|
胃腸功能改善
動物試驗
實驗設計:包含正常對照組、肥胖對照組及3個不同劑量組,每組至少8隻動物(小白鼠隻數每組至少10隻
促進消化吸收長期(4週以上)口服胃腸功能改善功效性試驗 |
|
改善腸內細菌菌相長期(4週以上)口服胃腸功能改善功效性試驗 |
|
幫助(改善)胃腸運動長期(4週以上)口服胃腸功能改善功效性試驗 |
|
有助於胃黏膜之保護作用長期(4週以上)口服胃腸功能改善功效性試驗 |
|
人體試驗
實驗設計:包含控制組及試驗組,每組人數至少為8人。
促進消化吸收實驗期至少2週 |
|
改善腸內細菌菌相實驗期至少2週 |
|
幫助(改善)胃腸運動實驗期至少2週 |
|
減少胃內幽門螺旋桿菌實驗期至少2週 |
|
輔助調整過敏體質功能
動物試驗
實驗設計:實驗組別每組至少10隻動物
針對一般過敏反應誘發過敏反應後,進行測試:小鼠 |
|
針對呼吸道過敏反應誘發過敏反應後,進行測試:小鼠 |
|
人體試驗
實驗設計:包含對照組及二至三組劑量的實驗組
|
建議由至少一家以上之試驗中心進行試驗以求公允 |
|
牙齒保健功能
動物試驗
實驗設計:包含對照組及實驗組,每組至少40隻動物。
|
二組之實驗鼠,皆應接種細菌,接種二天後,餵食測試物質:大鼠 |
|
人體試驗
實驗設計:包含對照組及實驗組,每組受試人數至少10人
|
不抽煙、無全身疾病、年齡為20至40歲之間且每毫升唾液中有105個以上之Streptococcus mutans之健康成人 |
|
骨質保健功能
動物試驗
實驗設計:包含對照組及2~3組不同劑量的實驗組,每組至少8隻動物(如使用實驗最終體重 < 250克之較小型動物時,每組至少12隻動物)
|
成長期 |
|
|
更年期卵巢切除 |
|
人體試驗
鈣質生物利用率測定受試者宜為健康之成年人,性別不拘,但女性受試者必須非懷孕、非授乳者 |
|
骨質變化測定
|
|
延緩衰老功能
動物試驗
老化動物之器官或組織老化包含對照組及應有3種不同劑量組(倘該類食品已有相關文獻或已有產品通過「健康食品」認證,則可採用2個劑量組),每組大鼠雌雄至少各8隻以上或每組小鼠雌雄至少各10隻以上
|
|
存活期試驗
|
|
人體試驗
實驗設計:包含安慰劑組及試驗組,實驗採雙盲交叉,實驗期之長短及服用時間自行視產品特性而擬定,但至少須≧12週
|
受試者必須為健康之成年人 (20-64歲與65歲以上,年齡相近,宜相差≦20歲) ,男女各10人以上(即共10×4=40人以上) |
|
促進鐵吸收功能
體外試驗
|
試驗動物採用原發性高血壓動物 |
|
動物試驗
實驗設計:包含低、中、高3種不同劑量組,每組至少8隻動物。
|
試驗動物採用原發性高血壓動物 |
|
人體試驗
實驗設計:包含對照組及實驗組,每組受試人數至少20人。
|
受試者為原發性高血壓患者,收縮壓介於130〜179 mmHg,舒張壓介於85〜109 mmHg,兩者有一項核實即可確診,且應本著自覺自願的原則。 |
|


